63家醫械機構被市場監管總局點名(附目錄)
醫藥網5月25日訊

63家機構進入名單
5月22日,國家市場監管總局更新公布獲國家級資質認定的醫療器械防疫用品檢驗檢測機構名錄。
據統計,這批機構共63家,均已通過國家認證認可監督管理委員會審批取得資質認定。
其中41家具有醫用一次性防護服檢測能力;43家具有醫用防護口罩檢測能力;38家具有醫用外科口罩檢測能力;35家具有一次性使用醫用口罩檢測能力;42家具有一次性使用滅菌橡膠外科手套檢測能力等。
除了公布檢驗檢測機構名單,國家市場監管總局還發通知表示,要嚴厲規范防疫用品的出口認證市場。
5月19日,國家市場監管總局發布《市場監管總局關于深入開展質量提升行動促進常態化疫情防控和全面復工復產達產的通知》,要求深入整頓和規范認證市場。
重點查處偽造、冒用、非法買賣認證證書和認證標志的違法行為,查處未經批準擅自在我國境內從事認證活動的違法行為,檢查認證機構認證活動不規范、認證價格違法等問題。
國內檢驗檢測機構良莠不齊
國際疫情持續接近3個月,目前對防疫物資的需求仍然居高不下,山東某科技有限公司相關負責人在疫情期間進入醫用口罩生產行業,他對賽柏藍器械表示,國際口罩市場仍然火熱,美國、俄羅斯、巴西、西班牙的口罩需求明顯較大。
“最近俄羅斯的客戶報過來需求,要200萬個一次性口罩和200萬個KN95口罩。”他說。
上述負責人供應的口罩同樣需要檢驗檢測,但是據表述,目前我國的檢驗檢測機構良莠不齊。
據介紹,檢驗檢測報告包括口罩的細菌指數、細菌過濾值、材質等多方面數據,一般用于和客戶溝通,讓客戶了解產品信息,但是國外有部分客戶不太認可這些檢測報告。
上述負責人對賽柏藍器械分析,不認可的原因有兩方面,第一是部分報告純中文,客戶閱讀不便,無法對信息進行核實;第二是國內的檢驗檢測機構良莠不齊。
“部分機構的數據并沒有那么準確,而且有不合法機構對數據造假,甚至淘寶里都有認證機構。”他說。
近日,國家市場監管總局發布的《市場監管總局“聯合雙打行動”典型案例(第十八批)》也顯示,有企業未經批準擅自開始認證活動。
2020年4月1日,廣東省廣州市番禺區市場監管局對廣東廣州市標達檢測技術有限公司開展執法檢查。經查,此公司分別于3月2日及3月6日出具虛假證書4張,獲利5000元。最終處以23萬元的行政處罰。
對于檢驗檢測的問題,上述負責人還對賽柏藍器械說到,有FDA認證或者CE認證后,出口會方便很多,但其中部分認證的費用高達200多萬,而且周期太長,一般6-9個月。
他還表示,目前國內有檢驗檢測需求的企業太多,但通過國家資質認定的檢驗機構偏少。
對于此類問題,今日國家市場監管總局發消息表示,除本次公布的63家檢驗檢測機構,全國還有253家獲得省級市場監管部門資質認定的防疫用品檢驗檢測機構,具體名單由各省、自治區、直轄市及新疆生產建設兵團市場監管局(廳、委)公布。
附件:








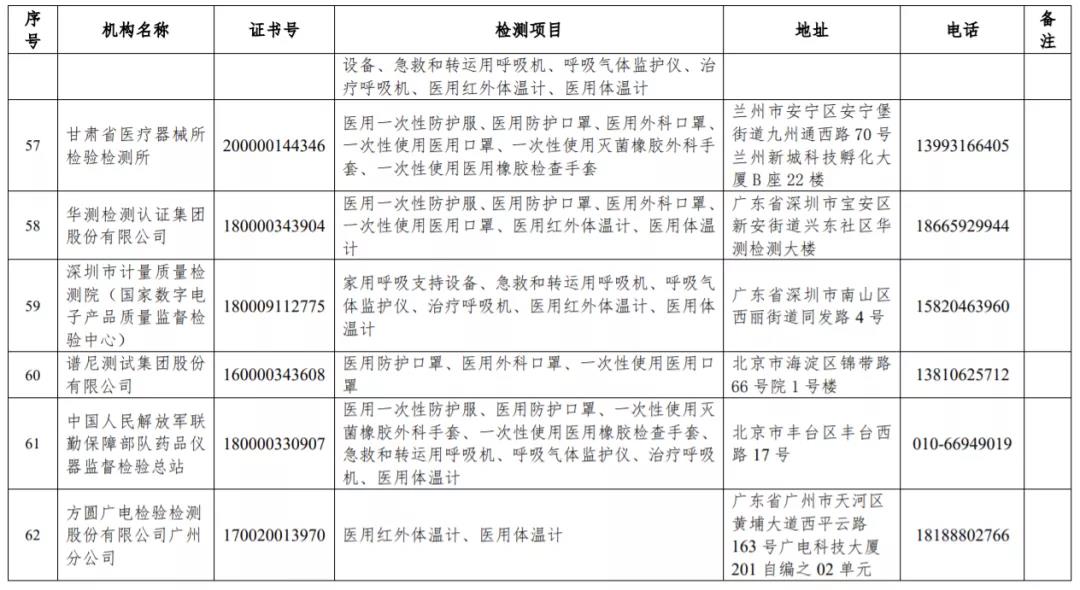

【來源:賽柏藍器械】







