5家械企,24款產品獲優先審批
發布時間:2018/2/5 9:09:54
2018年1月,依據《廣東省第二類醫療器械優先審批程序(試行)》要求,廣東省食品藥品監督管理局擬同意對這些第二類醫療器械進行優先審批。
優先審批的“好處”
對于獲批的醫療器械,食藥監受理、審評及許可部門,可以按照早期介入、專人負責、科學審批的原則,在標準不降低、程序不減少的前提下,對獲批醫療器械予以優先辦理,并加強與申請人的溝通交流。
這對申請人來講,無疑給產品注冊上市之路帶來極大的便利,甚至建立了一道與專家隨時溝通的VIP快速通道,相當于請了一個免費的權威軍師,大大有助于企業在初期研發設計、產品檢測、臨床試驗,以及過程中涉及到的體系核查、注冊資料編制、技術評審等多方面的疑難雜癥。
誰得此“特權”
一月份在廣東省獲得優先審批的總共有4家械企,分別是珠海市麗拓生物科技有限公司(2個產品)、珠海康德萊醫療器械有限公司(3個產品)、深圳市新產業生物醫學工程股份有限公司(16個產品)、廣州七喜醫療設備有限公司(1個產品)、深圳雷杜生命科學股份有限公司(2個產品)。
優先申報理由均為:上一年度被省局評為質量信用A類,且本年度不在生產整改或涉案處理期間,未有醫療器械質量公告不合格的醫療器械生產企業。
深圳市新產業生物醫學工程股份有限公司是獲得審批編號最多的廠家,它是專注于化學發光免疫分析領域研究的國家級高新技術企業。在去年7月份,成為中國第一家通過美國FDA認證的化學發光廠家。
廣東省2018年1月優先審批醫械產品表
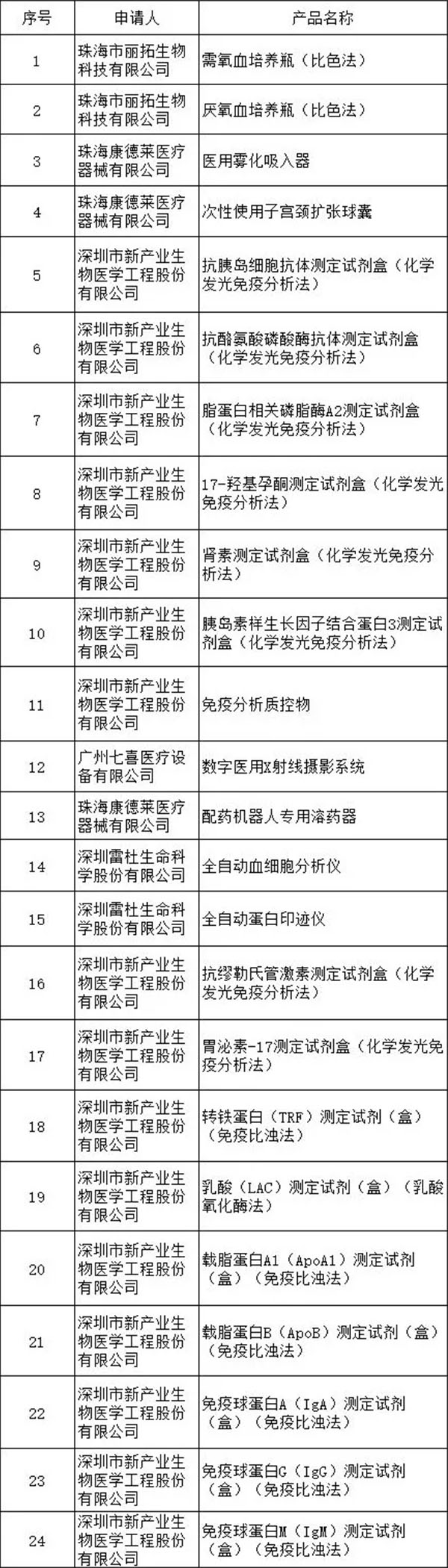
【來源:賽柏藍器械】







